
- =>Definir o seu processo de gerenciamento de risco
- =>Estabeleceras regras do gerenciamento e responsabilidades
- =>Documentar o plano de gerenciamento de risco
- =>Estabelecer um arquivo de gerenciamento de risco vivo

- =>Compreender e definir o escopo do seu dispositivo e documentar o uso pretendido

- =>Identificar as fontes potenciais de danos associados ao seu produto. Isto é conhecido como perigo

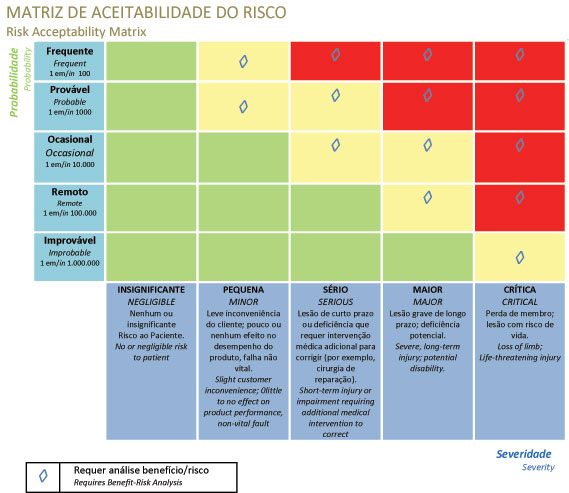
- =>Estimar risco de cada situação perigosa.

- =>Risco é a combinação de severidade do potencial dano e a probabilidade de ocorrência do dano

- =>Os riscos estão em um nível aceitável?
- =>É necessária a redução do risco?

- =>Use o controle de risco para reduzir o risco a níveis aceitáveis.
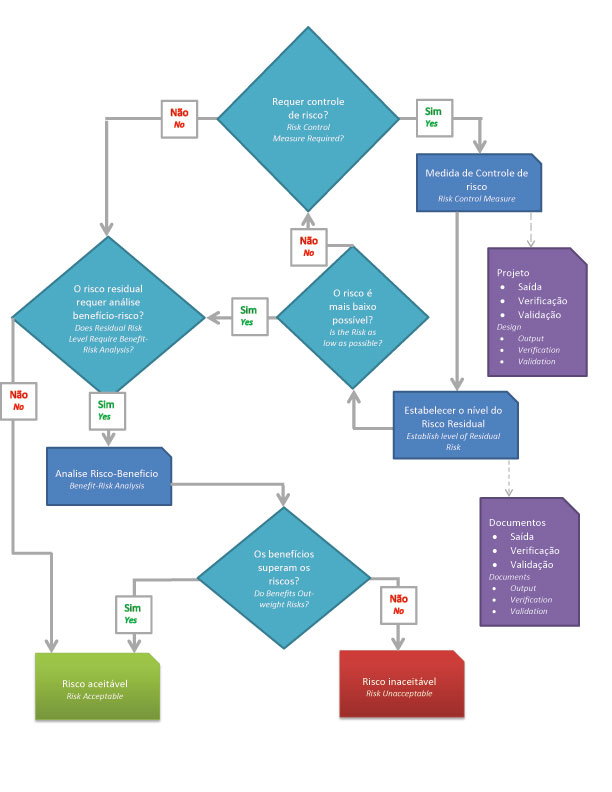

- =>Avalie o risco do produto em sua totalidade.
- =>O nível de risco é aceitável?
- =>O benefício superam os potencias riscos?

- =>Realize uma análise de gerenciamento de risco e prepare um relatório de gerenciamento de risco antes de enviar seu dispositivo para produção comercial.

- =>Auditoria internas, Ações preventivas e corretivas, conformidades, retorno de clientes, não conformidades de material, todos as fontes no processo de gerenciamento de risco.
- =>O gerenciamento de risco é um processo para todo o ciclo de vida do produto.
Na próxima publicação, escreverei sobre dicas práticas para uma boa reunião de análise de risco.Deixe seu comentário e até o próximo post.





